
PROCYSBI® er indisert for behandling av påvist nefropatisk cystinose. Reduserer cystinakkumulering i enkelte celler (f.eks. leukocytter, muskel- og leverceller) ved nefropatisk cystinose, og forsinker utvikling av nyresvikt når behandling påbegynnes på et tidlig stadium.1
Cystinkontroll med dosering to ganger daglig1,2
PROCYSBI er basert på enterodrasjerte perler med forsinket frisetting (DR=delayed release) av cysteaminbitartrat, der de mikrosfæriske perlene er ytterligere innkapslet i en hard gelatinkapsel for å muliggjøre oral administrering hver 12. time.3
Differensiell absorpsjon i tarmen muliggjør langvarig frigjøring av cysteamin og gir økt biotilgjengelighet av cysteamin.
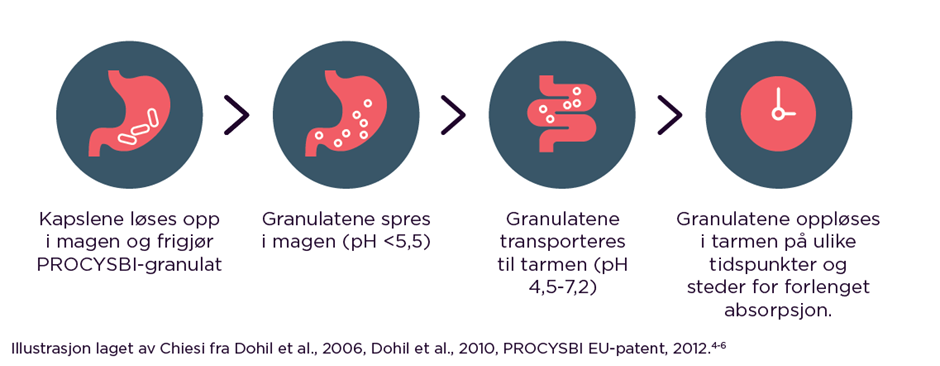
- En langsommere absorpsjon av cysteamin på grunn av formuleringen med forsinket frisetting av PROCYSBI driver farmakokinetikken og fører til en tilsvarende topp av cysteaminnivåer som for cysteamin med umiddelbar frisetting, men med forlenget platåtid.3
- PROCYSBI går forbi magen, noe som fører til vedvarende absorpsjon i tynntarmen7
- PROCYSBI gir 12 timers cystinkontroll og muliggjør dosering to ganger daglig1,3
Dosering: Behandling bør initieres under tilsyn av lege med erfaring med behandling av cystinose. Anbefalt dose avhenger av vekt/kroppsoverflate. Måldose for vedlikehold er 1,3 g/m2/dag, fordelt på 2 doser gitt hver 12. time. Maks. anbefalt dose er 1,95 g/m2/dag. Oppstartsdose for nylig diagnostiserte er 1/6-1/4 av måldosen for vedlikehold. Det skal tas regelmessige prøver for å måle leukocyttcystinkonsentrasjonen. Disse prøvene er med på å bestemme dosen og prøvene skal tas 12,5 timer etter kveldsdosen dagen før, dvs. 30 minutter etter den påfølgende morgendosen gis.
Administrering: Kapslene kan svelges hele, eller gis ved at innholdet i kapselen strøs over mat, væske eller gis gjennom en sonde. Hele kapsler skal ikke gis til barn <6 år pga. at kapslene kan sette seg fast i halsen. Måltider og meieriprodukter bør unngås i minst 1 time før og etter administrering.
Cysteaminbehandling bør settes i gang raskt så snart diagnosen er bekreftet (dvs. forhøyet WBC-cystin) for å oppnå maksimal nytte.1
PROCYSBI er tilgjengelig i 25 mg og 75 mg harde enterokapsler med cysteamin.1
Utvalgt sikkerhetsinformasjon1
- Kontraindikasjoner: Overfølsomhet overfor penicillamin. Amming.
- Alvorlige hudskader er sett. Rutinemessig overvåkning av hud og benvev anbefales. Hvis hud- eller benabnormiteter opptrer, skal dosen reduseres eller stoppes. Ved erythema multiforme bullosa/toksisk epidermal nekrolyse skal cysteamin ikke readministreres.
- Forsiktighet utvises ved tegn på gastrointestinale sår og blødninger. Kvalme, oppkast, anoreksi og magesmerter er forbundet med cysteamin. Fibroserende kolonopati skal utelukkes ved mindre vanlige/endring i symptomer.
- Anfall, somnolens, depresjon og encefalopati er forbundet med cysteamin. Hvis CNS-symptomer oppstår, bør pasienten vurderes nøye og dosen ev. justeres.
- Reversibel leukopeni og unormal leverfunksjon er sett. Blodverdier og leverfunksjon bør overvåkes.
- Leukocyttcystinnivået bør overvåkes nøye ved nedsatt nyre- eller leverfunksjon samt hos dialyse- eller posttransplanterte pasienter.
- Det er sett idiopatisk intrakranial hypertensjon/papillødem. For å unngå synstap er periodisk synsundersøkelse nødvendig for å identifisere og behandle tilstand tidlig.
- Ved samtidig bruk med bikarbonat, skal bikarbonat tas minst én time før eller etter Procysbi.
- Graviditet/Amming: Kvinner i fertil alder skal informeres om risiko for teratogenitet og rådes til å bruke prevensjon under behandling. En negativ graviditetstest skal bekreftes før behandlingsstart. Skal ikke brukes under graviditet, spesielt ikke under 1. trimester, hvis ikke strengt nødvendig. Kontraindisert under amming.
- Bivirkninger: Hyppigst sett er Anoreksi, oppkast, kvalme, diaré, letargi og feber.
Øvrig produktinformasjon
Procysbi (cysteamin (som merkaptaminbitartrat)), harde enterokapsler 25 mg og 75 mg
Pakninger og pris (AUP): 25 mg: 60 stk.: kr 5925,00. 75 mg: 250 stk.: kr 71.356,90. Reseptgruppe: C. Refusjon: H. Besluttet innført av Beslutningsforum 20.06.2022. LIS2199e.
For utfyllende informasjon om dosering, administrering, kontraindikasjoner, forsiktighetsregler, interaksjoner og bivirkninger, se Procysbi SPC godkjent 26.05.2023.
Klikk på produktnavnet for Felleskatalogtekst for Procysbi®
Referanser:
- Procysbi SPC
- Langman CB, Greenbaum LA, Grimm P, et al. Quality of life is improved and kidney function preserved in patients with nephropathic cystinosis treated for 2 years with delayed-release cysteamine bitartrate. J Pediatr. 2014;165(3):528-33.e1. doi:10.1016/j.jpeds.2014.05.013
- Langman CB, Greenbaum LA, Sarwal M, et al. A randomized controlled crossover trial with delayed-release cysteamine bitartrate in nephropathic cystinosis: effectiveness on white blood cell cystine levels and comparison of safety [published correction appears in Clin J Am Soc Nephrol. 2013 Mar 7;8(3):468]. Clin J Am Soc Nephrol. 2012;7(7):1112-1120. doi:10.2215/CJN.12321211
- Dohil R, Fidler M, Gangoiti JA, Kaskel F, Schneider JA, Barshop BA. Twice-daily cysteamine bitartrate therapy for children with cystinosis. J Pediatr. 2010;156(1):71-75.e753. doi:10.1016/j.jpeds.2009.07.016
- Dohil R, Rioux P. Pharmacokinetic Studies of Cysteamine Bitartrate Delayed-Release. Clin Pharmacol Drug Dev. 2013;2(2):178-185. doi:10.1002/cpdd.12
- European patent office, PROCYSBI patent EU EP1919458A2. 2012. https://patents.google.com/patent/EP1919458A2/zh: (Accessed 25.10.2024)
- Medic G, van der Weijden M, Karabis A, Hemels M. A systematic literature review of cysteamine bitartrate in the treatment of nephropathic cystinosis. Curr Med Res Opin. 2017;33(11):2065-2076. doi:10.1080/03007995.2017.1354288